Điều trị cấy ghép có thể gây nên viêm quanh implant, và không có phương pháp nào để điều trị phản ứng viêm này được xem là có hiệu quả. Gần như là không thể điều trị những bề mặt nhiễm trùng như TiUnite (một lớp màng Titan oxit) để kích tạo xương, thế nên nhưng việc tìm ra một phương pháp hiệu quả là vô cùng cần thiết. Nhiều thí nghiệm được thực hiện để xác định công suất chiếu xạ tối ưu để loại bỏ lớp oxit titan bị ô nhiễm bằng chiếu xạ laser Er: YAG, mức độ nóng lên của implant có phải do sự chiếu laser Er:YAG hay không, hay quá trình tích hợp xương liệu có diễn ra hay không theo sau sự nổ bọt vi thể laser Er:YAG nhằm loại bỏ lớp phủ bề mặt của những implants cắm trên chó becgie. Laser Er:YAG hiệu quả trong việc loại bỏ lớp titan oxit phẳng, và việc phun nước sẽ hạn chế sự tỏa nhiệt của implant được chiếu laser, do đó giúp bảo vệ mô xương xung quanh không bị phá hủy bởi nhiệt.Viêm quanh Implant có thể được điều trị hiệu quả bằng việc chiếu laser Er:YAG (Int J Periodontics Restorative Dent – Nha khoa phục hồi, tạp chí nha chu quốc tế 2013;33:21–29. doi: 10.11607/prd.1593)
1. Lecturer, The Japan Institute for Advanced Dental Studies (JIADS), Osaka and Tokyo, Japan; President, Perio-Implant Hospital AUTIS, Osaka, Japan.
2. Associate Professor, Department of Implantology, Division of Oral Pathogenesis and Disease, Asahi University School of Dentistry, Gifu, Japan.
Correspondence to: Dr Atsuhiko Yamamoto, 5-4-16 Fujisawadai, Tondabayashi, Osaka, Japan; fax: +81 721-29-4182; email: autis@silver.ocn.ne.jp.
©2013 by Quintessence Publishing Co Inc.
Mặc dù những implants đã tích hợp xương được chứng minh có tỷ lệ tồn tại cao, nhưng mô xung quanh chúng có thể bị tình trạng viêm tương tự như trong bệnh nha chu. Tình trạng viêm này có hai loại: Viêm niêm mạc quanh implant và viêm quanh immplant. Viêm niêm mạc quanh implant được định nghĩa là tình trạng viêm mô mềm quanh impant mà không gây tiêu xương nâng đỡ xung quanh. Viêm quanh implant bao gồm cả viêm mô mềm và tiêu xương nâng đỡ quanh implant. Viêm quanh implant xảy ra trên 28%-56% bệnh nhân vì chúng có liên quan đến nhiều yếu tố nguy cơ như: vệ sinh răng miệng kém, tiền sử viêm nha chu và hút thuốc lá. Hiện có nhiều phương pháp điều trị viêm quanh implant được đề ra, nhưng không có cách thức nào thực sự vượt trội. Nhiều loại lasers được dùng để điều trị viêm quanh implant nhưng chúng chỉ có tác dụng diệt khuẩn bề mặt chứ chưa loại bỏ được lớp màng nhiễm khuẩn. Và việc khử khuẩn bề mặt implant với laser Er:YAG chính là một phương pháp điều trị đầy hứa hẹn.
Gần đây, laser Er: YAG được sử dụng để điều trị viêm quanh implant mà không cần mở vạt. Sự viêm được điều trị bằng việc chiếu laser vào túi nha chu quanh implant. Tuy nhiên, phương pháp này chỉ điều trị viêm chứ không giải quyết được tác nhân gây viêm thực sự. Vì vậy, chưa có sự nhất trí về phương pháp tối ưu cho việc sử dụng laser Er:YAG trong điều trị viêm quanh implant. Nghiên cứu này nhằm để (1) xác định năng lượng chiếu tối ưu để lấy đi lớp oxit titan trên bề mặt bằng chiếu laser Er: YAG, (2) xác định mức độ nóng lên của implant gây ra do quá trinh chiếu, và (3) xác định xem sau khi lấy đi lớp bề mặt oxit titan ô nhiễm bằng sự vi nổ bọt của laser Er: YAG, quá trình tích hợp xương có thể xảy ra trên mô hình động vật được hay không .
Phương pháp và tư liệu nghiên cứu
Năng lượng chiếu tối ưu
Để xác định điều kiện chiếu tối ưu cho việc loại bỏ lớp titan oxit nhờ hơi nóng bằng laser Er: YAG (Erwin AdvErl, J. Mori- ta), những implants 15 3.75 × 13-mm Brånemark MkIII RP TiUnite được đem chiếu bằng đầu PS600T (J. Morita) với laser Er: YAG; tip thạch anh trơn loe có đường kính từ 600 μm ở phần trên đến 400 μm ở phần dưới. Dùng một pha điện X-Y được dùng (ALD- 904-H1, Chuo Precision Industrial) và được đặt ở tốc độ 0,2 mm/s. Khoảng cách từ đầu tip đến implant khoảng 0,05 mm.
Độ cắt bề mặt có công suất ở mức 50 mJ/mm2, 100 mJ/mm2, và 200 mJ/mm2 , năng lượng phát ra ở đầu dụng cụ được đo bằng đồng hồ đo công suất sẽ đáng tin hơn số liệu được hiển thị bởi máy laser, vì sợi dẫn sáng và đầu dụng cụ sẽ làm giảm một phần năng lượng của laser. Mỗi implant được thay một đầu tip mới, và năng lượng laser được đo cho từng lần một. Xung được đặt ở mức 20 PPS, nước được tiêm vào ở mức 5mL/giây, và thời gian chiếu là 15 giây. Những thay đổi trên bề mặt chiếu được kiểm tra bằng kính hiển vi quang học và kính hiển vi điện tử tương phản pha.
Sự nóng lên của implant
Phần cổ của implant 3.75 × 13-mm Bråne- mark MkIII RP TiUnite được gắn cố định vào tấm nhựa acrylic để mô phỏng các điều kiện lâm sàng. Sử dụng tia laser Er: YAG (Erwin AdvErl) với đầu tip PS600T, đầu implant được chiếu với năng lượng đầu ra là 100mJ (10 PPS) và 50mJ (20PPS) trong vòng 15s (tổng năng lượng là 1500mJ). Chiếu laser được thực hiện ngay cả khi có hoặc không có phun nước với tốc độ 5ml/phút.
Implant được chiếu dưới 4 kiểu : (1) có phun nước và mức năng lượng là 100mJ và 10 PPS, (2) không phun nước và mức năng lượng là 100mJ và 10PPS (3) có phun nước và mức năng lượng là 50 mJ và 20 PPS, (4) không phun nước và mức năng lượng là 50 mJ và 20 PPS. Nhiệt độ tăng lên được theo dõi bằng nhiệt ký (Neo Thermo TVS-700, Nippon Avionics).
Năm implants được làm nóng trong mỗi kiểu, được làm nguội đến nhiệt độ phòng (đo bằng nhiệt ký) và sau đó lại sử dụng để kiểm tra với kiểu tiếp theo. Sự gia tăng nhiệt độ được theo dõi bằng nhiệt kí thay vì cặp nhiệt điện, vì đo nhiệt độ bề mặt sẽ phản ảnh được nhiệt độ của phần tiếp xúc với tế bào xương và cũng bởi vì những thí nghiệm sơ bộ cho thấy nhiệt độ không thể đo chính xác bằng cặp nhiệt điện do tia laser Er: YAG cũng gây ra sự gia tăng nhiệt độ trong cặp nhiệt điện. Để so sánh mức tăng nhiệt giữa các loại laser khác nhau, một thí nghiệm riêng biệt đã được thực hiện bằng cách sử dụng laser carbon dioxide (CO2) (Laserwin, J. Morita). Thiết bị laser CO2 không được trang bị xịt hơi, vì vậy các tác giả đã thực hiện một thử nghiệm riêng biệt bằng cách sử dụng laser CO2 với thiết bị xịt hoặc không có thiết bị xịt. Sự tăng nhiệt khác nhau giữa các loại là khoảng 10 o C . Do vậy, người ta quyết định sử dụng laser CO2 không cần xịt hơi và ở dạng nguyên gốc , với một dòng khí làm mát là 260mL/phút
Sự tích hợp xương của những implants được chiếu laser lần đầu.
Tất cả răng cối đều được nhổ ở hai bên hàm dưới ở loài chó becgie, giống cái, 18 tháng tuổi. nặng khoảng 12 kg. Sau 3 tháng, chụp phim X quang để chắc chắn ổ nhổ răng đã lành thương đúng.

Hình 1a to 1c (a và b). Hình ảnh hiển vi điện tử tương phản pha. Lớp TiUnite được loại bỏ hoàn toàn bởi những bọt nổ vi thể. Bề mặt mới lộ ra không hề bị tan chảy hay biến dạng bởi hiệu ứng làm nóng của việc chiếu laser. Phần bên trái và bên trên thể hiện bề mặt trước khi chiếu laser Er:YAG, trong khi đóphần bên phải và phía dưới thể hiện bề mặt sau khi chiếu laser Er:YAG. (c) Implant với điều trị laser ở phần chóp.
Một máy laser Er:YAG được dùng để chiếu và quét đi một nửa bề mặt TiUnite implants 24 3.75 × 13-mm. Hai implant được cắm vào vị trí nhổ răng, với moment xoắn lúc đầu là 35-45 Ncm. Implant được đặt sau cho nửa chiếu nằm ở mặt má và một nửa không được chiếu nằm ở mặt lưỡi . 2 con vật đã bị giếtsau 2 tuần, sau 4 tuần giết thêm 2 , và 2 con cuối cùng bị giết sau 6 tuần. Mẫu mô được nhuộm với hematoxylin-eosin, không khử khoáng , để chuẩn bị làm mẫu quan sát. Hình ảnh với độ phóng đại 10 × và 200× được chụp ở mốc 2,4 và 6 tuần. Để giữ độ kiên định, hình ảnh được chụp ở độ phóng đại 200×, giữa ren thứ 4 và thứ 5
Kết quả
Năng lượng chiếu tối ưu
Tại 50mJ/mm2, lớp TiUnite không thể được loại bỏ hoàn toàn.Tại 100 mJ/mm2, lớp TiUnite bằng phẳngcũng được loại bỏ hiệu quả, và bề mặt lộ ra cũng không bị biến dạng do nóng chảy, do cacbon hóa, hay do những tác động khác của nhiệt (Hình 1). Tại 200 mJ/mm2, lớp TiUnite và cả lớp titan bên dưới bị nóng chảy.
Kết quả trong Hình 2.
Khi implant được chiếu với laser Er: YAG có phun nước làm mát, thì nhiệt độ tăng lên tối đa 3oC cho cả 2 kiểu ( 100mJ ở 10 PPS và 50mJ ở 20PPS). Tuy vậy khi dùng dạng laser này mà không phun nước, nhiệt độ của đầu implant tăng từ 30-33oC ở 100 mJ
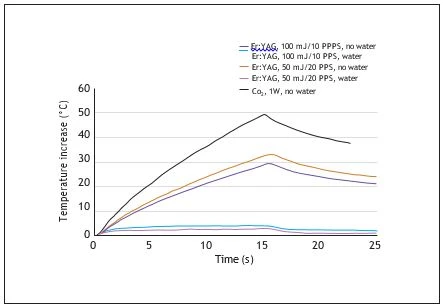
Hình 2: Nhiệt độ tăng lên khi chiếu laser. Kết quả biểu diễn tia laser Er:YAG được sử dụng cùng với phun nước để điều trị viêm quanh implant.
10PPS, 330C ở 50 mJ và 20 PPS.
Chiếu Laser CO2 làm tăng nhiệt độ đầu implant lên đến 50oC, mặc dù đã sử dụng hệ thống làm mát không khí ở lưu lượng tối đa.
Tích hợp xương ở implants vừa được chiếu laser.
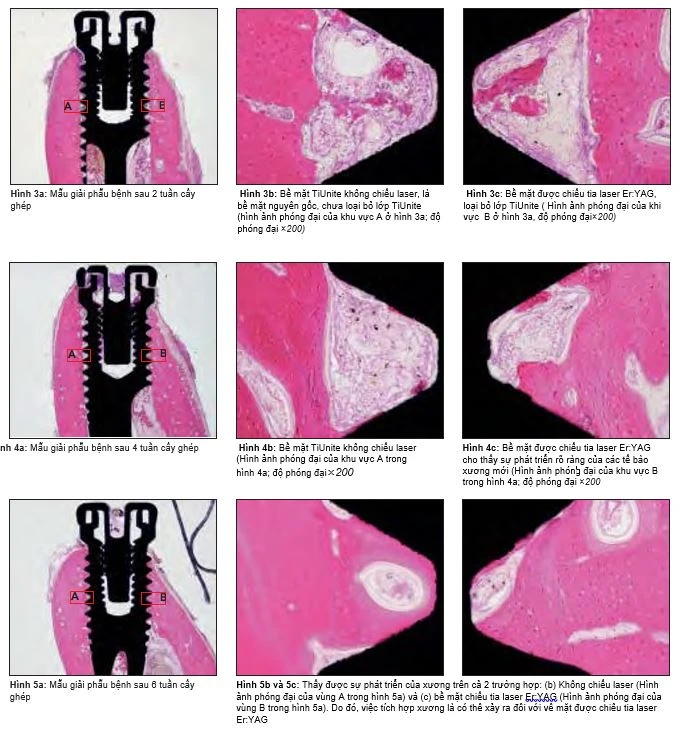
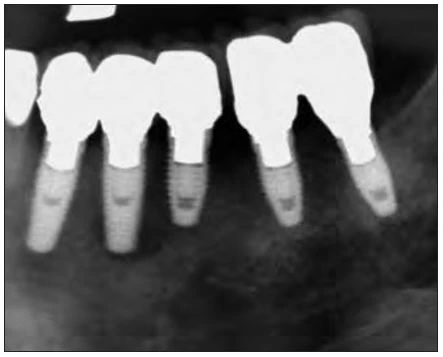
Hình 3a đến 3c cho thấy implant sau 2 tuần ở độ phóng đại 10× và 200×. Sự xâm nhập nhẹ của mô dạng xương được ghi nhận trên cả bề mặt không chiếu laser (Hình 3b) và bề mặt chiếu laser (Hình 3c). Hình 4a đến 4c cho thấy implant sau 4 tuần ở độ phóng đại 10× và 200×
Mô dạng xương được hình thành trên bề mặt không chiếu laser (Hình 4b), và mô dạng xương cũng hình thành dọc bề mặt implant chiếu laser và lấp đầy một phần ba khoảng trống (Hình 4c). Hình 5a đến 5c cho thấy implant sau 6 tuần ở độ phóng đại 10× và 200×. Xương hình thành được thấy trên cả bề mặt không chiếu (Hình 5b) và bề mặt được chiếu laser (Hình 5c).
Bàn luận
Năng lượng chiếu tối ưu
Nếu chất đáng nghi có cấu trúc dạng hang (cavelike) tương tự TiUnite, thì trên lý thuyết, tia laser có thể loại bỏ vi khuẩn và tạp chất bên trong nó.
Tuy vậy, tia laser với chùm tia chiếu thẳng sẽ khó xâm nhập và những cấu trúc không đều. Vì vậy, nhiều tác giả cho rằng việc loại bỏ lớp TiUnite (lớp Titan oxit nhiễm khuẩn) là rất cần thiết. Tia laser Er:YAG có mức độ hấp thu lớn nhất với nước-gấp gần 10 lần so với laser CO2, gần 70,000 lần so với laser Nd:YAG, và gần 600,000 lần so với laser diode. Khi năng lượng tia laser Er:YAG được hấp thu bởi nước, nước lập tức bị bốc hơi. Thể tích nước tăng lên gấp 1000 lần , dẫn đến tình trạng nổ vi thể. Nhiều tác giả tin rằng hiệu ứng này giúp ích trong điều trị viêm quanh implant. Những phát hiện này cho thấy răng: sử dụng năng lượng với công suất nhỏ hơn 100mJ/mm2 có thể hiệu quả trong việc khử khuẩn bề mặt, lớp TiUnite sẽ được loại bỏ hoàn toàn bởi những vụ nổ vi thể từ tia laser Er:YAG
Hình 6: X quang cho thấy vùng tiêu xương đáng kể quanh implants ở phía sau góc phần tư bên trái của xương hàm dưới.
Sự nóng lên của implant
Boulnois18 phát hiện ra rằng các tế bào sẽ bắt đầu biến dạng và chết ở nhiệt độ giữa 43oC và 45oC, protein sẽ thoái hóa và đông lại ở 60oC. Mặc dù tia laser CO2 từng được báo cáo là chỉ được hấp thu rất ít bởi titan và không gây ra sự thay đổi hình thái bề mặt, nhưng những kết quả gần đây cho thấy việc chiếu tia laser CO2 lên implant có thể làm nóng nó đến mức đủ để gây hoại tử mô xương. Chiếu tia laser Er:YAG kèm phun nước cũng có thể gây phá hủy tương tự.
Tuy nhiên, việc phun nước giúp sự tỏa nhiệt giảm tối đa và không dẫn đến tình trạng phá hủy không hồi phục.
Sự tích hợp xương trên implants vừa chiếu laser.
Những thí nghiệm trên động vật cho thấy sự tích hợp xương xảy ra trên bề mặt sạch, không nhiễm khuẩn nhờ chiếu tia laser. Hơn nữa, Kreisler et al 10 báo cáo rằng bề mặt implant được tiệt khuẩn bởi tia laser Er:YAG. Những kết quả trên đã thừa nhận mạnh mẽ rằng khó khăn trong điều trị viêm quanh implants có thể vượt qua được nhờ tia laser Er:YAG, vì chúng có thể lấy đi lớp titan oxit nhiễm khuẩn và tạo ra bề mặt implant sạch, được khử khuẩn mà không phá hủy các ren của implant. Bề mặt mới này dường như cũng có các đặc tính cảm ứng tạo xương với hiệu quả tương tự bề mặt TiUnite ban đầu (không chiếu tia)
.
Clinical case Ca lâm sàng
.
Ca lâm sàng dưới đây mô tả về việc sử dụng tia laser Er:YAG để điều trị một bệnh nhân bị viêm quanh implant.
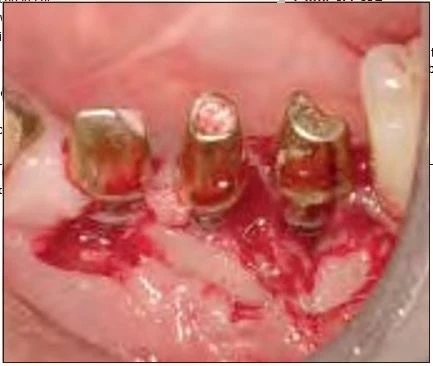
Hình 7: Sau khi lật vạt phía má, một lượng lớn mô hạt viêm được lấy ra bởi tia laser Er:YAG
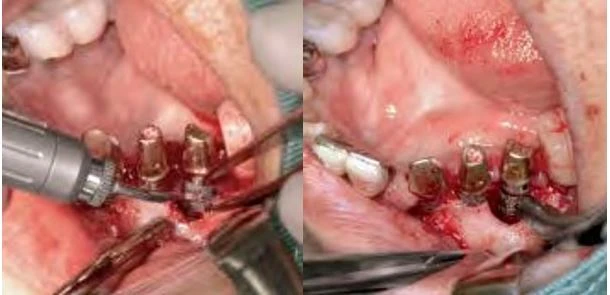
Hình 8a và 8b: Chìa khóa để lấy đi được mô hạt nhiễm khuẩn bằng laser Er:YAG là không chiếu laser vào chính khối mô hạt mà phải chiếu laser vào nơi giao nhạu giữa mô hạt và mô xương lành. Bằng cách này, mô hạt nhiễm khuẩn có thể được lấy đi trọn một khối duy nhất. Sau khi loại bỏ mô hạt, bề mặt nhiễm khuẩn TiUnite được lấy đi và được tiệt khuẩn.
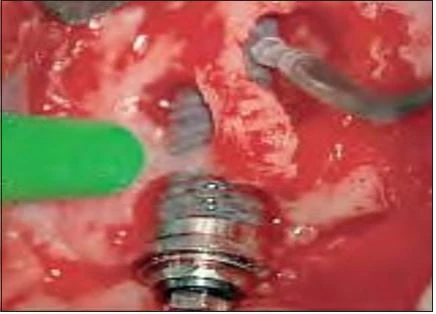
Hình 9: Sử dụng tia laser Er:YAG kèm theo phun nước giúp implant tránh khỏi sự nóng lên quá mức. Những vụ nổ vi thể được tạo ra khi laser tác động vào nước, chúng giúp loại bỏ máu và những vật cản thấy được
Vào tháng chín 2006, một phụ nữ 81 tuổi được cấy tổng cộng chín implants, năm trong số chúng được thể hiện trong hình 6: vị trí răng nanh trái hàm dưới, răng cối nhỏ thứ nhất và thứ hai, răng cối lớn thứ nhất và thứ hai. Sau 4 tháng, phục hình tạm được thực hiện, và sau 6 tháng bệnh nhân được mang phục hình chính thức. Sau 1 năm, bệnh nhân than phiền về tình trạng sưng tấy quanh implant. Kiểm tra X quang cho thấy tình trạng tiêu xương đáng kể quanh implants ở vùng phần tư phía sau hàm dưới bên trái (Hình 6). Khi cấu trúc trên cùng bị loại bỏ, người ta phát hiên ra rằng implants không hề bị lỏng. Tuy nhiên, tình trạng viêm đã lan sang viêm-đây là một trường hợp rõ ràng của viêm quanh implant tiến triển. Những kiểm tra khác xác định rằng đây là một ca CIST (liệu pháp hỗ trợ ngăn chặn tích tụ – cumulative interceptive supportive therapy) loại D ( độ sâu túi > 5mm, có chảy máu khi thăm khám, và tiêu xương > 2mm). Sau khi tiêm thuốc tê tại chỗ (2% xylocaine), vạt phía má được lật lên ở vị trí phần tư hàm dưới trái. Tuy implants không bị lỏng, nhưng lại thấy tình trạng tiêu xương đáng kể và sự hình thành mô hạt (Hình 7). Mô hạt nhiễm khuẩn được cắt bỏ và lấy đi bằng tia laser với đầu PS600T ở năng lượng 50mJ và 20 PPS kèm với phun nước tiệt trùng ở lưu lượng 5mL/min (Hình 8a và 8b). Mô hạt thường được loại bỏ bằng nạo, nhưng máu chảy ra do nạo làm vùng điều trị không được nhìn rõ ràng. Sử dụng tia laser Er:YAG cùng phun nước để loại bỏ vấn đề này. Việc áp dụng phun nước và những sự nổ vi thể (xảy ra khi tia laser bắn vào nước) sẽ giúp giữ cho vùng làm việc luôn được nhìn thấy rõ ràng.
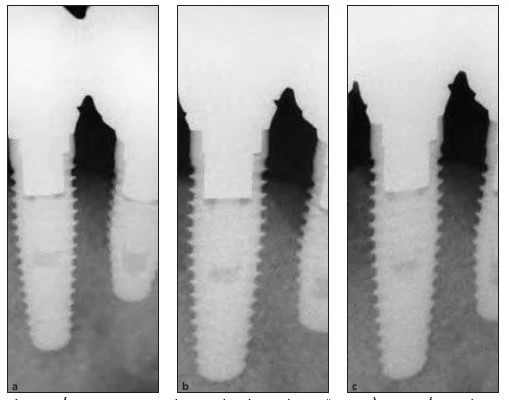
Hình 10a đến 10c: X quang chụp lúc (a) 3 tháng và (b) 2 và (c) 3 năm sau điều trị cho thấy sự phát triển xương ổn định.
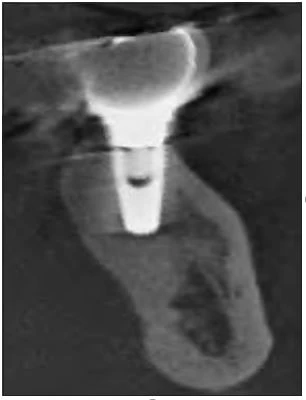
Hình 11: Chụp cắt lớp vi tính sau 4 năm điều trị. Viêm quanh implant được giải quyết, và khu vực quanh implant đã ổn định .
Sau khi lấy đi mô hạt nhiễm khuẩn, bề mặt implant nhiễm khuẩn được tiệt trùng bằng cách lấy đi lớp bề mặt TiUnite. Một đầu PS600T được hướng dẫn di chuyển nhẹ trên bề mặt ở năng lượng 50 mJ và 20 PPS với lưu lượng phun nước là 5mL/phút. Lớp nhiễm khuẩn được lấy đi nhờ các bọt nổ vi thể gây ra bởi phản ứng của tia laser Er:YAG với nước.
Vùng xám hơi tối có thể được thấy trên bề mặt đã được cắt bỏ lớp nhiễm khuẩn, đây không phải là kết quả của quá trình carbon hóa và đó là bề mặt của titan mới. Implants thường được đặt chiều thẳng đứng, và khi tia laser chiếu vuông góc với implant, chúng có thể chạm tới từng chi tiết của các ren và tiệt trùng triệt để lớp titan oxit nhiễm khuẩn bằng cách lấy đi từng lớp một. Một mảnh xương ghép tự thân được cấy vào và che lại bằng màng tự tiêu, sau đó vị trí này được đóng lại theo cách thông thường.
Phim X quang được chụp lúc 3 tháng, 2 năm và và 3 năm sau phẫu thuật (Hình 10a đến 10b),tất cả chúng đều có thấy sự tái tạo xương rõ rệt. Chụp cắt lớp vi tính (lát cắt má lưỡi) được chụp sau 4 năm điều trị (hình 11). Vùng xung quanh implant đã ổn định.
Kết luận
Những bọt nổ vi thể tạo bởi tia laser Er:YAG có thể lấy đi một cách hiểu quả lớp titan oxit nhiễm khuẩn trên implant (chính là implant bị thất bại do viêm quanh Implant)
Chiếu tia laser Er:YAG kèm với phun nước sẽ hạn chế sự nóng lên của implant đến vài độ, và ở nhiệt độ này không đủ để gây phá hủy mô xương xung quanh hay ức chế sự tích hợp xương. Những báo cáo từ các thí nghiệm trên động vật cho thấy sự tích hợp xương có thể xảy ra trên bề mặt sạch (được tạo ra bởi chiếu tia laser)
Lời cảm ơn
Các tác giả xin cảm ơn các bác sĩ Yoshi-hiro Ono, Yasukazu Miyamoto, Toshiaki Yo-shino và Akira Aoki vì đã tiếp tục hỗ trợ nghiên cứu. Các tác giả không có xung đột lợi ích liên quan đến nghiên cứu này.
Tư liệu
1. van Winkelhoff AJ. Consensus on peri- implant infections [in Dutch]. Ned Tijd- schr Tandheelkd 2010;117:519–523.
2. Zitzmann NU, Berglundh T. Definition and prevalence of peri-implant diseas- es. J Clin Periodontol 2008;35(suppl): 286–291.
3. Schou S, Berglundh T, Lang NP. Surgical treatment of peri-implantitis. Int J Oral Maxillofac Implants 2004;19:140–149.
4. Claffey N, Clarke E, Polyzois I, Renvert S. Surgical treatment of peri-implantitis. J Clin Periodontol 2008;35(suppl):316–332.
5. Ungvári K, Pelsöczi IK, Kormos B, et al. Effects on titanium implant surfaces of chemical agents used for the treatment of peri-implantitis. J Biomed Mater Res B
6. Appl Biomater 2010;94:222–229.
7. Persson GR, Samuelsson E, Lindahl C, Renvert S. Mechanical non-surgical treatment of peri-implantitis: A single- blinded randomized longitudinal clinical study. II Microbiological results. J Clin Periodontol 2010;37:563–573.
8. Schwarz F, Sahm N, Iglhaut G, Becker J. Impact of the method of surface de- bridement and decontamination on the clinical outcome following combined surgical therapy of peri-implantitis: A ran- domized controlled clinical study. J Clin Periodontol 2011;38:276–284.
9. Persson LG, Ericsson I, Berglundh T, Lindhe J. Osseointegration following treatment of peri-implantitis and re- placement of implant components. An experimental study in the dog. J Clin Periodontol 2001;28:258–263.
10.Deppe H, Horch HH, Henke J, Donath K. Peri-implant care of ailing implants with the carbon dioxide laser. Int J Oral Maxil- lofac Implants 2001;16:659–667.
11. Kreisler M, Kohnen W, Marinello C, et al. Bactericidal effect of the Er:YAG laser on dental implant surfaces: An in vitro study. J Periodontol 2002;73:1292–1298.
12. Renvert S, Lindahl C, Roos Jansåker AM, Persson GR. Treatment of peri-implanti- tis using an Er:YAG laser or an air-abra- sive device: A randomized clinical trial. J Clin Periodontol 2011;38:65–73.
13. Stubinger S, Etter C, Miskiewicz M, et al. Surface alterations of polished and sandblasted and acid-etched titanium implants after Er:YAG, carbon dioxide, and diode laser irradiation. Int J Oral Maxillofac Implants 2010;25:104–111.
14. Badran Z, Bories C, Struillou X, Saffarza- deh A, Verner C, Soueidan A. Er:YAG la- ser in the clinical management of severe peri-implantitis: A case report. J Oral Im- plantol 2011;37(spec no):212–217.
15. Takasaki AA, Aoki A, Mizutani K, Kiuchi S, Oda S, Ishikawa I. Er:YAG laser therapy for peri-implant infection: A histological study. Lasers Med Sci 2007;22:143–157.
16. Schwarz F, Sculean A, Rothamel D, Schwenzer K, Georg T, Becker J. Clinical evaluation of an Er:YAG laser for nonsur- gical treatment of peri-implantitis: A pi- lot study. Clin Oral Implants Res 2005;16: 44–52.
17. Schwarz F, Bieling K, Sculean A, Herten M, Becker J. Treatment of periimplantitis with laser or ultrasound. Areview of the lit- erature [in German]. Schweiz Monatsschr Zahnmed 2004;114:1228–1235.
18. Schwarz F, Bieling K, Bonsmann M, Latz T, Becker J. Nonsurgical treatment of moderate and advanced periimplantitis lesions: A controlled clinical study. Clin Oral Investig 2006;10:279–288.
19. Boulnois JL. Photophysical processes in recent medical laser development. La- sers Med Sci 1986;1:47–66.
Biên Dich: Công ty Anh & Em
Bài đăng lần đầu ngày: 24 Tháng 6, 2019 @ 3:32 chiều




